Inzulín: Porovnání verzí
Značka: editace z Vizuálního editoru |
|||
| Řádek 41: | Řádek 41: | ||
=== '''Působení inzulínu'''<big></big> === | === '''Působení inzulínu'''<big></big> === | ||
| − | Inzulín je anabolický hormon, jehož úkolem je snižování hodnoty glykémie tím, že glukózu z krve dostává do cílových buněk, které mají pro Inzulín specifický receptor. Nejtypičtějšími cílovými buňkami pro Inzulín jsou buňky tkáně svalové, jaterní a tukové.<ref>Yang, Z., Scott, C., Mao, C., Tang, J., & Farmer, A. (2014). Resistance Exercise Versus Aerobic Exercise for Type 2 Diabetes: A Systematic Review and Meta-Analysis. Sports Medicine, 44(4), 487-499. </ref> Inzulín tedy působí anabolicky tím, že podporuje tvorbu tuků a ukládání glukózy do zásoby ve formě svalového a jaterního glykogenu. <ref>Despopoulos, A., & Silbernagl, S. (2003). Color atlas of physiology (5. vyd., s. 282). Germany: Wemding.</ref> V cílových tkáních se Inzulín váže na membránové receptory, které tvoří 2 α-podjednotky na vnější straně membrány a 2 β-podjednotky procházející membránou. Jakmile se Inzulín naváže na receptor, dochází ke kaskádovité reakci fosforylací, které vedou k zabudování glukózových transportérů do plazmatických membrán cílových buněk. Glukózové transportéry (zejména skupina GLUT transportérů s označením GLUT-1 až GLUT-13) poté přenášení glukózu do buněk. <ref>Kittnar, O., Jandová, K., Kariščák, E., Langmeier, M., Marešová, D., Mlček, M., Mysliveček, J., Pokorný, J., Riljak, V., & Trojan, S. (2011). Lékařská fyziologie. (1. vyd., s. 526). Praha: Grada.</ref>[[Soubor:Působení Inzulínu na cílovou buňku.jpg|Působení Inzulínu na cílovou buňku]] | + | Inzulín je anabolický hormon, jehož úkolem je snižování hodnoty glykémie tím, že glukózu z krve dostává do cílových buněk, které mají pro Inzulín specifický receptor. Nejtypičtějšími cílovými buňkami pro Inzulín jsou buňky tkáně svalové, jaterní a tukové.<ref>Yang, Z., Scott, C., Mao, C., Tang, J., & Farmer, A. (2014). Resistance Exercise Versus Aerobic Exercise for Type 2 Diabetes: A Systematic Review and Meta-Analysis. Sports Medicine, 44(4), 487-499. </ref> Inzulín tedy působí anabolicky tím, že podporuje tvorbu tuků a ukládání glukózy do zásoby ve formě svalového a jaterního glykogenu. <ref>Despopoulos, A., & Silbernagl, S. (2003). Color atlas of physiology (5. vyd., s. 282). Germany: Wemding.</ref> V cílových tkáních se Inzulín váže na membránové receptory, které tvoří 2 α-podjednotky na vnější straně membrány a 2 β-podjednotky procházející membránou. Jakmile se Inzulín naváže na receptor, dochází ke kaskádovité reakci fosforylací, které vedou k zabudování glukózových transportérů do plazmatických membrán cílových buněk. Glukózové transportéry (zejména skupina GLUT transportérů s označením GLUT-1 až GLUT-13) poté přenášení glukózu do buněk. <ref>Kittnar, O., Jandová, K., Kariščák, E., Langmeier, M., Marešová, D., Mlček, M., Mysliveček, J., Pokorný, J., Riljak, V., & Trojan, S. (2011). Lékařská fyziologie. (1. vyd., s. 526). Praha: Grada.</ref>[[Soubor:Působení Inzulínu na cílovou buňku.jpg|Působení Inzulínu na cílovou buňku|400x400px]] |
Verze z 30. 11. 2014, 15:10
Obsah
Zařazení Inzulínu
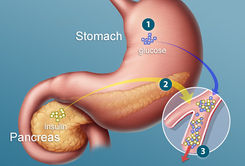
Inzulín je hormonem slinivky břišní. Slinivka břišní (Pancreas), je smíšenou žlázou s exokrinní (pars exocrina pancreatis) a endokrinní (pars endocrina pancreatis) částí. Exokrinní část pankreatu produkuje pankreatickou trávicí šťávu. [1] Endokrinní část je tvořena asi 1-2 miliony drobných, 0,1-0,5 mm velkých, buněčných okrsků, označovaných jako Langerhansovy ostrůvky, které jsou roztroušeny v exokrinní tkáni pankreatu. Langerhansovy ostrůvky tvoří asi 1,5 % objemu celé slinivky břišní. [2] Langerhansovy ostrůvky tvoří a uvolňují hormony do krevního řečiště a skládají se ze 4 typů sekrečních buněk. [3]
- A-buňky produkují hormon Glukagon (svým účinkem je antagonistou Inzulínu)
- B-buňky produkují hormon Inzulín
- D-buňky produkují hormon Somatostatin (snižuje produkci Inzulínu i Glukagonu)
- F-buňky produkují Pankreatický polypeptid (jeho funkce je zatím nejasná) [4]
Středem každého ostrůvku potom prochází kapilára, do jejiž krve se přímo vylučují vytvořené hormony. [5]
Charakteristika Inzulínu
Lidský Inzulín je proteohormon, složený z 51 aminokyselin. Aminokyseliny Inzulínu jsou organizovány do dvou polypeptidových řetězců A a B, navzájem spojených dvěma disulfidickými můstky. Gen pro Inzulín je kódován na 11. chromozomu. [6] 
Mechanismus Inzulínu
Vznik Inzulínu
Inzulín se tvoří právě v B-buňkách, které představují zhruba 60 % buněk Langerhansových
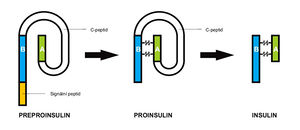
ostrůvků. Samotná tvorba potom probíhá v ribozomech (vznik preprohormonu Preproinzulínu) a v endoplazmatickém retikulu (vznik prohormonu Proinzulínu). Dále se v Golgiho aparátu vytvořený Inzulín s fragmenty peptidů zabuduje do sekrečních váčků, odkud je spolu s malým množstvím Proinzulínu (který nemá biologický účinek) vylučován do krve. [7]
Regulace sekrece Inzulínu
Inzulín se uvolňuje v tzv. pulzních dávkách, avšak trvale po celých 24 hodin denně. Důvod, proč se Inzulín uvolňuje trvale, je potřeba udržení citlivosti inzulínového receptoru a potlačení jaterní glukoneogeneze v podmínkách nalačno. Hlavním sekretagonem Inzulínu je glukóza, jejíž koncentrace v hodnotách 5,5-17,0 mmol/l krve vyvolá účinnou sekreci Inzulínu. [8] Tedy hlavním podnětem pro sekreci Inzulínu je zvýšení krevní glykémie. [9] Po jídle začíná stoupat sekreci Inzulínu již do 10 minut. [10] Stimulace B-buněk k vyloučení inzulínu probíhá v tomto sledu:
- Vzrůst plazmatické glukózy.
- Nárust glukózy v B-buňce pankreatu (Langerhansových ostrůvků).
- Zrychluje se oxidace již zvýšené hladiny glukózy v B-buňkách.
- To vede k nárustu koncentrace ATP v B-buňce.
- ATP-řízené draslíkové kanály se zavírají.
- Nastává depolarizace B-buňky.
- Potenciálem řízené vápníkové kanály se otevírají.
- Vzrůstá koncentrace vápníkových iontů v B-buňce.
- Nárust vápníkových iontů v B-buňce vyvolá exocytózu Inzulínu.
- Dochází ke znovuotevření draslíkových kanálů .
- Repolarizace B-buňky (návrat do výchozího stavu).[11]
Působení inzulínu
Inzulín je anabolický hormon, jehož úkolem je snižování hodnoty glykémie tím, že glukózu z krve dostává do cílových buněk, které mají pro Inzulín specifický receptor. Nejtypičtějšími cílovými buňkami pro Inzulín jsou buňky tkáně svalové, jaterní a tukové.[12] Inzulín tedy působí anabolicky tím, že podporuje tvorbu tuků a ukládání glukózy do zásoby ve formě svalového a jaterního glykogenu. [13] V cílových tkáních se Inzulín váže na membránové receptory, které tvoří 2 α-podjednotky na vnější straně membrány a 2 β-podjednotky procházející membránou. Jakmile se Inzulín naváže na receptor, dochází ke kaskádovité reakci fosforylací, které vedou k zabudování glukózových transportérů do plazmatických membrán cílových buněk. Glukózové transportéry (zejména skupina GLUT transportérů s označením GLUT-1 až GLUT-13) poté přenášení glukózu do buněk. [14]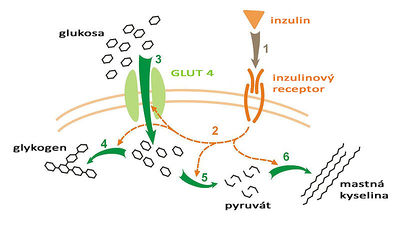
Odbourávání inzulínu
Poločas Inzulínu je 5-8 minut, přičemž je odbouráván hlavně v játrech, svalech a ledvinách. [15] Nejvšší degradece inzulínu je však způsobena inzulinázou v játrech a to až v míře 50 %. [16]
Odkazy
Reference
- ↑ Přidalová, M., Riegrová, J. (2009). Funkční anatomie II. (1. vyd., s. 93). Olomouc: Hanex.
- ↑ Čihák, R. (2013) Anatomie II. (3. vyd., s. 135). Praha: Grada.
- ↑ Kittnar, O., Jandová, K., Kariščák, E., Langmeier, M., Marešová, D., Mlček, M., Mysliveček, J., Pokorný, J., Riljak, V., & Trojan, S. (2011). Lékařská fyziologie. (1. vyd., s. 526). Praha: Grada.
- ↑ Patton, K. & Thibodeau, G. (2010). Anatomy & physiology (7. vyd., s. 563). USA.
- ↑ Kittnar, O., Jandová, K., Kariščák, E., Langmeier, M., Marešová, D., Mlček, M., Mysliveček, J., Pokorný, J., Riljak, V., & Trojan, S. (2011). Lékařská fyziologie. (1. vyd., s. 526). Praha: Grada.
- ↑ Piťhová, P., & Štechová, K. (2009). Léčba inzulínovou pumpou pro praxi (1. vyd., s. 13). Semily: Geum.
- ↑ Kittnar, O., Jandová, K., Kariščák, E., Langmeier, M., Marešová, D., Mlček, M., Mysliveček, J., Pokorný, J., Riljak, V., & Trojan, S. (2011). Lékařská fyziologie. (1. vyd., s. 526). Praha: Grada.
- ↑ Piťhová, P., & Štechová, K. (2009). Léčba inzulínovou pumpou pro praxi (1. vyd., s. 13). Semily: Geum.
- ↑ Despopoulos, A., & Silbernagl, S. (2003). Color atlas of physiology (5. vyd., s. 282). Germany: Wemding.
- ↑ Kittnar, O., Jandová, K., Kariščák, E., Langmeier, M., Marešová, D., Mlček, M., Mysliveček, J., Pokorný, J., Riljak, V., & Trojan, S. (2011). Lékařská fyziologie. (1. vyd., s. 526). Praha: Grada.
- ↑ Despopoulos, A., & Silbernagl, S. (2003). Color atlas of physiology (5. vyd., s. 282). Germany: Wemding.
- ↑ Yang, Z., Scott, C., Mao, C., Tang, J., & Farmer, A. (2014). Resistance Exercise Versus Aerobic Exercise for Type 2 Diabetes: A Systematic Review and Meta-Analysis. Sports Medicine, 44(4), 487-499.
- ↑ Despopoulos, A., & Silbernagl, S. (2003). Color atlas of physiology (5. vyd., s. 282). Germany: Wemding.
- ↑ Kittnar, O., Jandová, K., Kariščák, E., Langmeier, M., Marešová, D., Mlček, M., Mysliveček, J., Pokorný, J., Riljak, V., & Trojan, S. (2011). Lékařská fyziologie. (1. vyd., s. 526). Praha: Grada.
- ↑ Despopoulos, A., & Silbernagl, S. (2003). Color atlas of physiology (5. vyd., s. 282). Germany: Wemding.
- ↑ Kittnar, O., Jandová, K., Kariščák, E., Langmeier, M., Marešová, D., Mlček, M., Mysliveček, J., Pokorný, J., Riljak, V., & Trojan, S. (2011). Lékařská fyziologie. (1. vyd., s. 526). Praha: Grada.